第4章栄養と免疫,および生体防御機構
4-2:消化管と免疫
■概論
腸管は,腸蠕動や腸絨毛・粘液の被覆によるバリアー構造,粘液内のchemical agentsによる抗菌活性,マクロファージによる貪食などにより,外界からの細菌や毒素の体内への侵入を阻止している(図Ⅰ).腸管は,腸管関連リンパ組織(gut-associated lymphoid tissue:GALT)を有し,絶えず膨大な種類と量の異物(細菌,ウイルス,食物性タンパクなど)にさらされている.腸管は,安全な食物ならば生命維持に必要なものとして受け入れて体内に取り込み,病原性のある細菌は可及的すみやかに排除する識別機構を備えており,第二の脳(the second brain)ともよばれている.
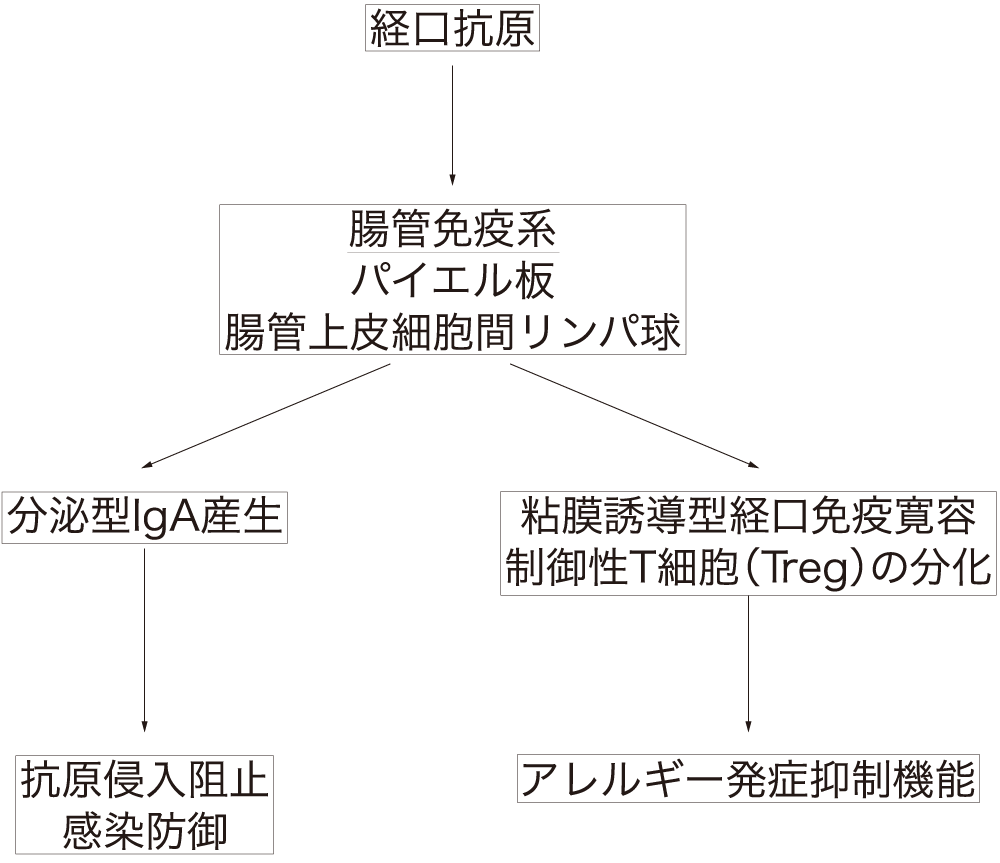
図Ⅰ●腸管免疫系
腸管免疫系では,経口抗原に対してパイエル板および腸管上皮細胞間リンパ球において抗原に特異的な反応をきたす.原菌が侵入した場合にはIgA が産生され,防御する.
また粘膜誘導型経口免疫寛容ではアレルギー発症抑制に関与している.
腸管免疫系を構成しているのは小腸上皮細胞,粘膜固有層,腸粘液層,パイエル板,孤立リンパ小節(isolated lymphoid follicles:ILFs),粘膜固有層リンパ球(lamina propria lymphocytes:LPLs),腸管上皮細胞間リンパ球(intraepithelial lymphocytes:IELs),腸間膜リンパ節,クリプトパッチ(cryptopatch:CP),形質細胞(plasma cell),マクロファージ,樹状細胞,好酸球,マスト細胞である(参考文献4-2-1).IELs,LPLsに存在するCD4+T細胞とCD8+T細胞を合わせた数は,全免疫系細胞のおおよそ60%を占めるともいわれる.これらのCD4+T細胞とCD8+T細胞は,経口的に体内に取り込まれる多量の抗原がM細胞を通過した後に抗原提示細胞により抗原提示されると,パイエル板における分泌型IgAの産生とともに生体防御の最前線として重要な役割を担っている.
分泌型IgAは,粘膜固有層の形質細胞により産生されて粘膜を介して腸管内に分泌される.殺菌作用は認めないが,毒素の中和や抗ウイルス抗体,抗細菌抗体など遮断抗体活性を示し,病原体やアレルゲンの腸管粘膜からの侵入を阻止する,感染防御に重要な免疫グロブリンである.感染は侵入性の細菌やウイルスなどの微生物が標的細胞(上皮細胞)の表面に接着することから開始されるが,分泌型IgAはこれらの微生物と特異的に結合することで微生物が上皮細胞に接着するのを阻止する.また,分泌型IgAは細菌が産生する毒素に対しても中和作用を示し,さらに食物中に含まれるアレルゲンと結合して食事性抗原の体内への吸収を阻止している.
一方で,食事性抗原にアレルギー反応や拒絶反応を起こさせないようにする抗原特異的な免疫学的無反応(粘膜誘導型経口免疫寛容)もまた腸管免疫機構の特徴の1つである(参考文献4-2-2)~(参考文献4-2-4).経口摂取されたタンパク抗原に対して,腸管において,Th1細胞,活性化マクロファージ,NK細胞のサイトカイン合成をブロックする合成抑制因子のIL-10や抑制性サイトカインのTGF-βを高産生するTreg細胞がパイエル板内に誘導され,経口免疫寛容における重要な役割を担っている(参考文献4-2-5),(参考文献4-2-6).免疫系を正常に保つにはTh2/Th1バランスが重要で,Th1細胞が多いと自己免疫疾患となる可能性が高くなり,Th2細胞が優位だとアレルギー疾患が起こりやすいといわれている.Tregは両方の過剰な産生を抑制し,免疫寛容を調節する.
 製品情報
製品情報
 よくあるご質問
よくあるご質問
 ご家庭向け製品情報
ご家庭向け製品情報
 医療機関・介護従事者向け情報
医療機関・介護従事者向け情報
 企業情報
企業情報
 公式通販
公式通販

![嚥下障害と誤嚥性肺炎[学ぶ&ケア]](/images/b_aside_nav_dysphagia.jpg)



![ご自宅で介護する方へ あなたの「おやっ?」は、床ずれのサインかも[学ぶ&ケア]](/top_new/images/recommend/p_recommend_pressureulcer.jpg)

![嚥下障害と誤嚥性肺炎[学ぶ&ケア]](/top_new/images/recommend/p_recommend_03.jpg)








